Công ty Roussel Việt Nam vừa bị xử phạt vì sản xuất thuốc không đảm bảo tiêu chuẩn có lai lịch như thế nào?
PLBD - Là doanh nghiệp nhà nước từng nhiều lần bị xử phạt do vi phạm liên quan đến sản xuất thuốc không đảm bảo tiêu chuẩn chất lượng, Công ty Roussel Việt Nam có thực sự đạt “tiêu chuẩn quốc tế” như quảng cáo?
Công ty Roussel Việt Nam là một doanh nghiệp nhà nước, trực thuộc Công ty TNHH MTV Dược Sài Gòn (SAPHARCO), có địa chỉ tại số 01, Đường số 3, Khu công nghiệp Việt Nam-Singapore, thị xã Thuận An, tỉnh Bình Dương do ông Lê Việt Hùng làm Giám đốc.
Công ty này có Giấy chứng nhận đủ điều kiện kinh doanh dược số 139/ĐKKDD-BYT do Bộ Y tế cấp ngày 14/11/2018.

Cục quản lý Dược (Bộ Y tế) vừa ra quyết định xử phạt Công ty Roussel Việt Nam do sản xuất thuốc Cortibion và Dumver có thay đổi lớn so với hồ sơ đăng ký thuốc đã được phê duyệt.
Công ty Roussel Việt Nam được thành lập vào năm 1959 dựa trên cơ sở liên doanh giữa Công ty Dược phẩm Roussel Uclaf (Pháp) và một số cổ đông ở Sài Gòn (nay là TP Hồ Chí Minh). Đến năm 1979, được ủy quyền của Bộ Y tế, Công ty Roussel Uclaf và Tổng Công ty Dược Việt Nam đã ký thỏa thuận liên doanh, trong đó Tổng Công ty Dược Việt Nam nắm giữ 51% vốn, phần còn lại thuộc về Roussel Uclaf.
Năm 1982, Bộ Y tế đã bàn giao phần vốn liên doanh cho UBND TP Hồ Chí Minh. Năm 1993, được ủy quyền của UBND TP Hồ Chí Minh, một hợp đồng liên doanh mới được ký kết giữa Roussel Uclaf và Công ty Dược Sài Gòn (nay là Công ty TNHH MTV Dược Sài Gòn-SAPHARCO). Năm 2003, Bộ Kế hoạch và Đầu tư đã ký quyết định chuyển Roussel Việt Nam từ liên doanh trở thành doanh nghiệp nhà nước trực thuộc Công ty TNHH MTV Dược Sài Gòn (SAPHARCO) và sau đó là doanh nghiệp trực thuộc hệ thống Công ty Mẹ - Con của công ty này.

Lễ khánh thành nhà máy Roussel Việt Nam tại tỉnh Bình Dương năm 2009
Năm 2009 công ty này khánh thành nhà máy đầu tiên tại KCN VSIP tỉnh Bình Dương. Nhà máy Roussel Việt Nam được xây dựng trên diện tích 10.000m2 do Công ty mẹ – Dược Sài Gòn (SAPHARCO) đầu tư với tổng kinh phí trên 120 tỷ đồng với các phân xưởng thuốc viên, bột, kem, nước; được quảng cáo với dây chuyền sản xuất công nghệ hiện đại từ châu Âu và Nhật Bản như: máy ép vỉ Đức, máy đóng thuốc COMAS hoàn toàn tự động.
Ông Lê Việt Hùng, Giám đốc Công ty Roussel Việt Nam từng phát biểu với báo chí về cam kết đảm bảo giá trị cốt lõi: "Chất lượng quốc tế; Uy tín khẳng định; Năng động, sáng tạo, nhân ái" và mục tiêu trong thời gian tới của Roussel Việt Nam là trở thành một trong những doanh nghiệp dược phẩm hàng đầu Việt Nam và trong khu vực vào năm 2020.

Ông Lê Việt Hùng, Giám đốc Công ty Roussel Việt Nam
Tuy nhiên, song hành với chặng đường hơn 60 năm phát triển, Công ty Roussel Việt Nam cũng không ít lần bị cơ quan chức năng "xướng tên" do vi phạm về sản xuất thuốc.
Tháng 1/2013, lô thuốckháng sinh Azissel 250 (Azithromycin 250mg) do Công ty Roussel Việt Nam sản xuất bị Cục Quản lý Dược đình chỉ lưu hành và thu hồi vì không đạt tiêu chuẩn chất lượng về chỉ tiêu độ hòa tan theo tiêu chuẩn cơ sở.
Tháng 8/2018, Công ty này tiếp tục bị yêu cầu đình chỉ lưu hành, thu hồi toàn quốc thuốc Rusartin 80mg, SĐK VD-11322-10 vì sản xuất từ nguyên liệu Valsartan do Trung Quốc cung cấp chứa tạp chất N-nitrosodimethylamine (NDMA) có thể gây ung thư.
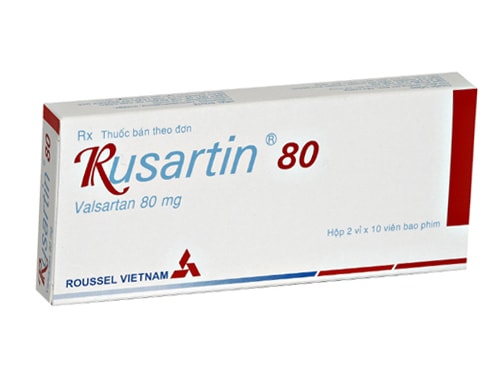
Thuốc Rusartin 80mg do Công ty Roussel Việt Nam sản xuất bị đình chỉ lưu hành và thu hôi do chứa tạp chất có thể gây ung thư.
Và gần đây nhất là ngày 31/12/2020, Cục Quản lý Dược (Bộ Y tế) đã ra Quyết định xử phạt Công ty Roussel Việt Nam tổng cộng 100 triệu đồng do hành vi sản xuất thuốc Cortibion (SĐK: VD-21043-14) và thuốc Dumver (SĐK: VD-32345-19) có thay đổi lớn so với hồ sơ đăng ký thuốc đã được phê duyệt nhưng chưa được phê duyệt nội dung thay đổi theo quy định của pháp luật quy định tại Điểm đ Khoản 3 Điều 57 của Nghị định 117/2000/NĐ-CP ngày 28/9/2020 của Chính phủ quy định về xử phạt vi phạm hành chính trong lĩnh vực y tế.
Với nhiều vi phạm liên quan đến việc sản xuất thuốc không đảm bảo tiêu chuẩn chất lượng như nêu trên, liệu Roussel Việt Nam có xứng đáng là một trong những doanh nghiệp dược phẩm hàng đầu Việt Nam và trong khu vực? Hay xứng đáng với "tiêu chuẩn quốc tế" và slogan "chung tay vì sức khỏe" mà công ty này đang quảng cáo?
